Ordinacija
Lijek ‘remdesivir’ za liječenje covida-19 čeka odobrenje za širu primjenu
4 min čitanja

“Iako još nema odobrenje za stavljanje u promet u EU-u, bolesnicima je dostupan kroz klinička ispitivanja te u sklopu milosrdnog davanja lijekova”
Europska agencija za lijekove (EMA) zaprimila je zahtjev za davanje uvjetnog odobrenja za stavljanje u promet (engl. conditional marketing authorisation, CMA) protuvirusnog lijeka remdesivir za liječenje bolesti COVID-19 te je formalno započela s njegovom ocjenom, prenosi Hrvatska agencija za lijekove i medicinske proizvode HALMED.
Ocjena koristi i rizika primjene remdesivira provodi se u skraćenom vremenskom roku te bi mišljenje moglo biti izdano u razdoblju od nekoliko tjedana, ovisno o kvaliteti dostavljenih podataka te mogućoj potrebi za dodatnim informacijama.
Tako kratak vremenski okvir moguć je zato što su određeni podaci već ocijenjeni tijekom prvog ciklusa postupne ocjene koji je započeo 30. travnja, a zaključen je 15. svibnja 2020. godine. Tijekom prve faze znanstvena povjerenstva i radne skupine pri EMA-i su kroz koordinirano djelovanje dovršila ocjenu dokumentacije znatno ranije nego u usporedbi s redovitim postupkom, uz istovremeno osiguravanje kvalitetne evaluacije dostupnih podataka.
Tekst se nastavlja ispod oglasa
Joker 15
Tijekom postupne ocjene, Povjerenstvo za humane lijekove (engl. Committee for Medicinal Products for Human Use, CHMP) pri EMA-i ocijenilo je podatke o kakvoći i proizvodnji, preliminarne podatke iz nekoliko kliničkih studija i prateće podatke iz programa milosrdnog davanja. Na kraju prvog ciklusa postupne ocjene CHMP je pozvao podnositelja zahtjeva da dostavi dodatne podatke zajedno sa zahtjevom za davanje uvjetnog odobrenja za stavljanje lijeka u promet.
Povjerenstvo za ocjenu rizika na području farmakovigilancije (engl. Pharmacovigilance and Risk Assessment Committee, PRAC) usporedno je dovršilo inicijalnu ocjenu preliminarnog plana upravljanja rizikom (engl. risk management plan, RMP) koji je predložio podnositelj zahtjeva, a koji predviđa mjere za prepoznavanje, karakterizaciju i minimiziranje rizika primjene lijeka. PRAC će i dalje ubrzano ocjenjivati sigurnosne podatke za remdesivir, kako bi brzo identificirao i adresirao moguća sigurnosna pitanja.
Povjerenstvo za pedijatriju (PDCO) pri EMA-i ubrzano je izdalo mišljenje o planu pedijatrijskog ispitivanja (engl. paediatric investigation plan, PIP) u kojem je opisano kako lijek treba razviti i proučiti za primjenu u djece, u skladu s ubrzanim rokovima za lijekove za COVID-19, te je odluka usvojena.
Tekst se nastavlja ispod oglasa
Ako dodatni podaci u zahtjevu za uvjetno odobrenje budu dostatni za zaključak CHMP-a kako koristi primjene lijeka remdesivir nadmašuju njegove rizike u liječenju bolesti COVID-19, EMA će usko surađivati s Europskom komisijom kako bi podržala ubrzanje procesa donošenja odluka i davanje odobrenja za stavljanje lijeka u promet od strane Europske komisije koje je valjano u svim državama članicama Europske unije i državama Europskog gospodarskog prostora.
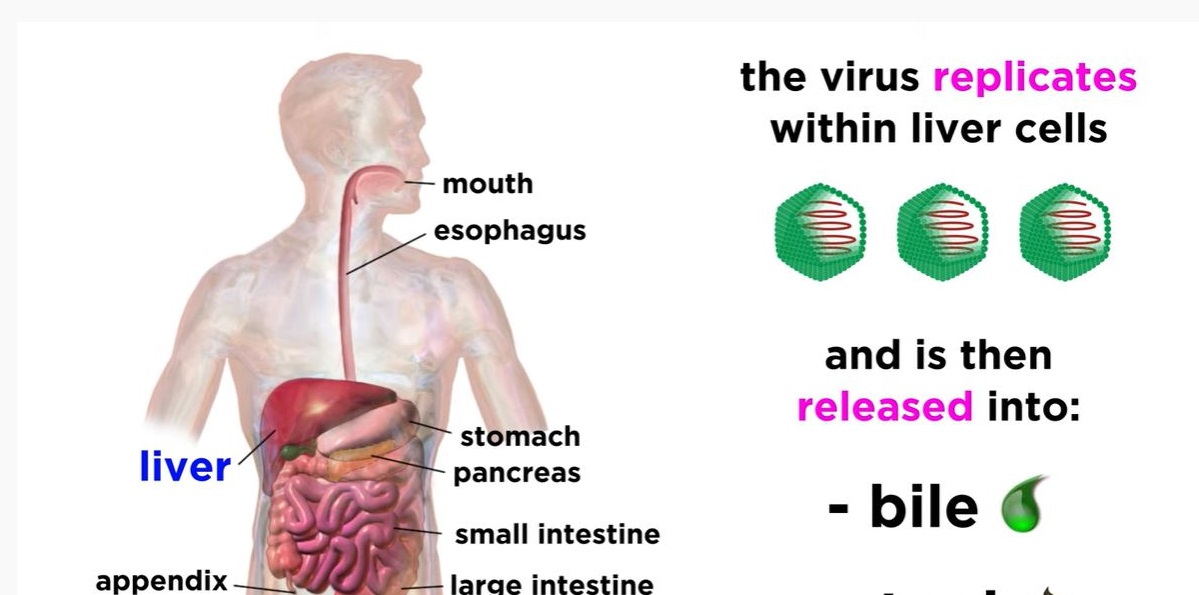
Remdesivir je protuvirusni lijek koji se istražuje za liječenje bolesti COVID-19. Remdesivir je inhibitor virusnog enzima RNA polimeraze (lijek koji ometa stvaranje virusnog genetskog materijala, sprječavajući umnožavanje virusa). Pokazao je in vitro aktivnost protiv različitih RNA virusa, uključujući virus SARS-CoV-2 te je prvotno razvijen za liječenje bolesti uzrokovane virusom ebole.
Iako remdesivir još nema odobrenje za stavljanje u promet u EU-u, bolesnicima je ovaj lijek dostupan kroz klinička ispitivanja te u sklopu milosrdnog davanja lijekova.
Tekst se nastavlja ispod oglasa
Remdesivir razvija tvrtka Gilead Sciences, Inc. te se primjenjuje infuzijom (drip) u venu, objašnjavaju iz HALMED-a.
D.H.
Doktore, hitno!